
Service Hotline
400-685-1800

前言
微透析技术是一种体内采样技术,它通过结合灌流与透析原理,实现对组织间质液或血液间质成分的动态采集。该技术能够实时监测细胞代谢、炎症反应及组织活力,为生命科学研究和药物评价提供了有力工具。
药代动力学(PK)运用动力学原理与数学模型,定量描述药物在体内的吸收、分布、代谢和排泄过程,进而预测药物浓度变化并指导剂量方案设计。传统的药代动力学研究通常需在多个时间点采集组织样本,操作繁琐且难以反映局部药物的动态变化。相比之下,微透析技术具有显著优势:它能够实时、连续地监测局部组织中游离药物的浓度变化,采样过程对组织损伤小,并可实现局部给药。这些特点使其在药代动力学-药效学(PK-PD)整合研究中展现出重要价值[1-2]。
微透析原理介绍
微透析(microdialysis, MD)是一种基于透析原理的活体采样技术。其核心机制为:在非平衡条件下,组织中的待测物沿浓度梯度扩散至植入组织的微透析探针中,随后被持续流动的灌流液带出,从而实现从活体组织中连续、动态取样[3-4]。
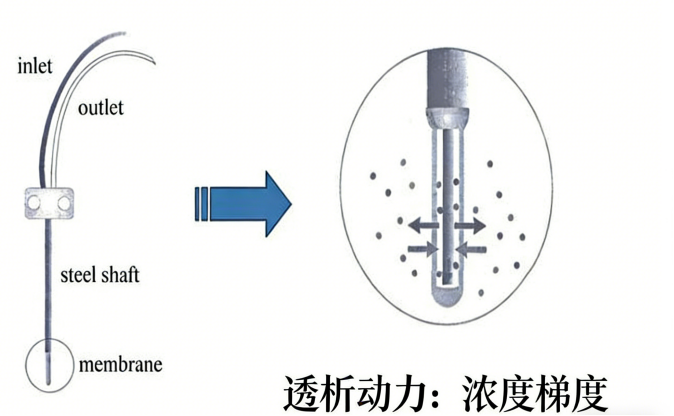
图1 微透析技术原理示意图
微透析取样组成
微透析系统通常由微透析探针、连接管路、样品收集器和微量注射泵构成。其中,探针是系统的关键部件,其技术发展推动了微透析在多领域的应用。

图2 微透析取样各部分组成示意图
微透析取样实验实施之前我们最先需要确定的是所使用的探针类型。
1、首先确定实验动物种类(大鼠、小鼠、猴、兔等),不同动物所适配的微透析探针类型存在差异。
2、明确目标透析部位,包括脑、血液、皮肤、肝脏、肾脏、关节等,其中脑部为最常用的透析部位,可选用专用脑部探针;其他组织则根据其结构与特性,分别选用血液探针或线性探针。
3、确定探针膜长度:微透析探针采用半透膜结构,具有固定规格。脑部探针膜长分为 1 mm、2 mm、3 mm、4 mm 四种,主要依据目标脑核团大小进行选择;血液探针又称柔性探针,膜长分为 4 mm 和 10 mm 两种,多用于外周组织透析,选择同样取决于目标透析区域的大小。
4、确定探针膜的分子截留量:分子截留量反映半透膜孔径大小,单位为道尔顿(Da)。以 20000 Da 为例,仅允许分子量小于 20000 Da 的物质通过自由扩散进入膜内,而蛋白质、多肽等大分子物质无法透过。因此,微透析技术所采集的样品可直接用于高效液相色谱检测,不易造成色谱系统堵塞。
目前常用的探针类型主要包括:
1、同心圆探针:主要用于脑部等组织;
2、柔性探针:适用于血液、肝脏等组织;
3、线性探针:适用于肌肉、皮肤、肿瘤等外周组织。
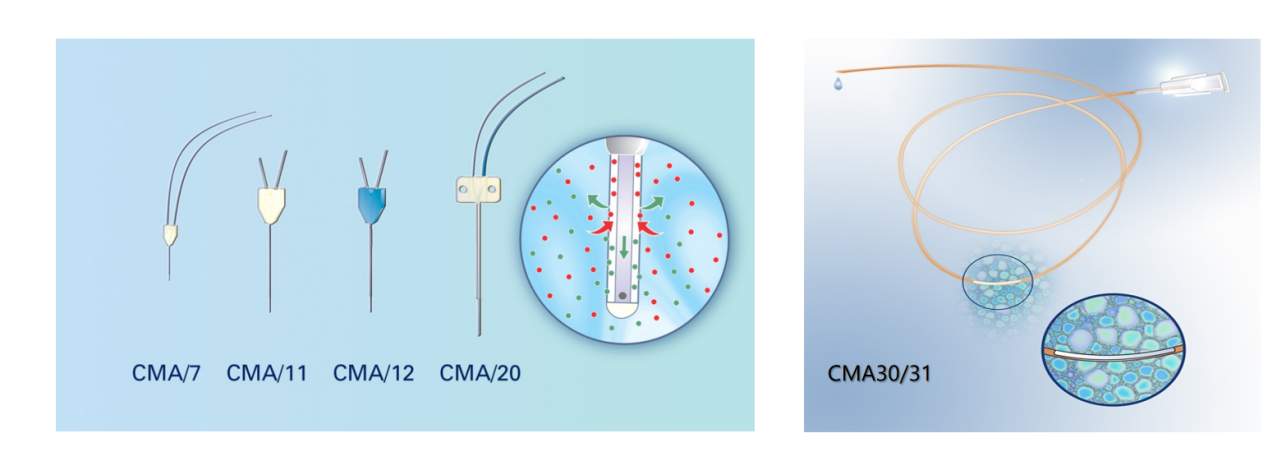 图3 微透析探针示意图
图3 微透析探针示意图
微透析技术的优点
基于其独特的工作原理,微透析技术具备以下突出优点:
1、实时性与动态性:可连续监测生命过程的动态变化;
2、多部位同步采样:支持同一动物不同器官或同一器官不同区域的同步采样,实现自身对照,提升实验效率与数据可靠性;
3、微创采样:取样量小,对机体生理状态干扰轻微;
4、样品处理简便:所获样品无需复杂前处理,可直接用于液相色谱或质谱分析,减少误差;
5、样品纯净稳定:样品中不含大分子蛋白质与酶,不易降解,便于保存与分析;
6、兼具给药功能:探针可作为局部给药途径,使药物直接作用于靶组织,提升药动与药效研究的整合水平。
微透析技术的应用领域
作为一项经典的活体采样技术,微透析已广泛应用于药物体内外药代动力学研究。早期主要应用于脑部,随着技术发展,其采样部位已扩展至心、肝、肺、肾、皮肤、小肠及血液等多种组织。目前,该技术在药理学、神经科学及生物医学等领域受到高度重视[5-6]。
微透析技术应用案例
1、脑部微透析
脑组织是微透析技术应用最早且最为成熟的领域。借助专用于自由活动动物的微透析系统(如北京铭泰佳信科技有限公司产品),现已能在大鼠、小鼠等清醒动物脑内实现连续采样。传统脑组织匀浆法需处死动物,无法在同一动物中观察药物浓度的经时变化,导致数据存在时空局限性。脑微透析技术则能在清醒动物上实时监测脑组织细胞外液中游离药物及其代谢产物的动态变化,为研究药物跨血脑屏障(BBB)的转运机制提供了关键手段。
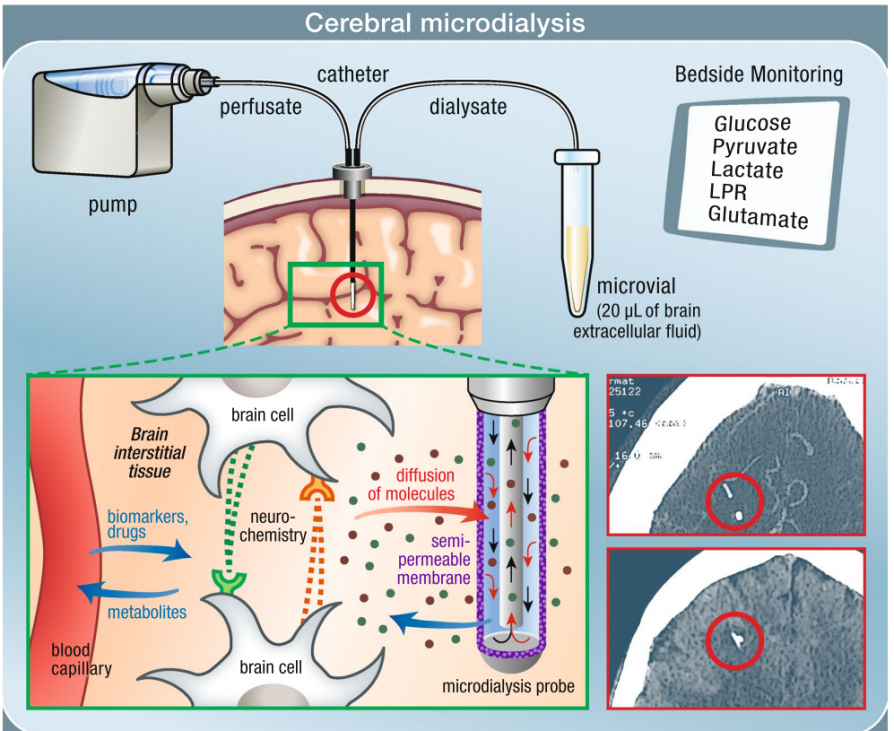
图4 脑微透析采样过程示意图[7]
在药代动力学研究中,Kp,uu(组织中游离药物浓度与血浆中游离药物浓度的比值)是评估药物脑内分布的关键参数,可用于判断药物跨BBB的转运特性[8](如表1)
其中“C”表示浓度(Concentration)。
下标“b”代表脑(brain),“p”代表血浆(plasma)。
下标“u”代表未结合(unbound),即游离状态、未与蛋白质(如白蛋白)结合的药物。
表1,基于Kp,uu的药物转运机制评估
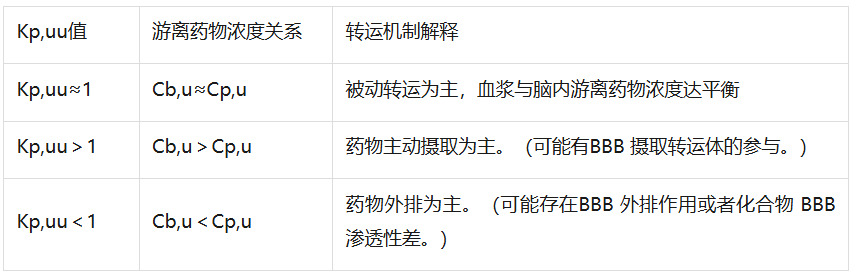
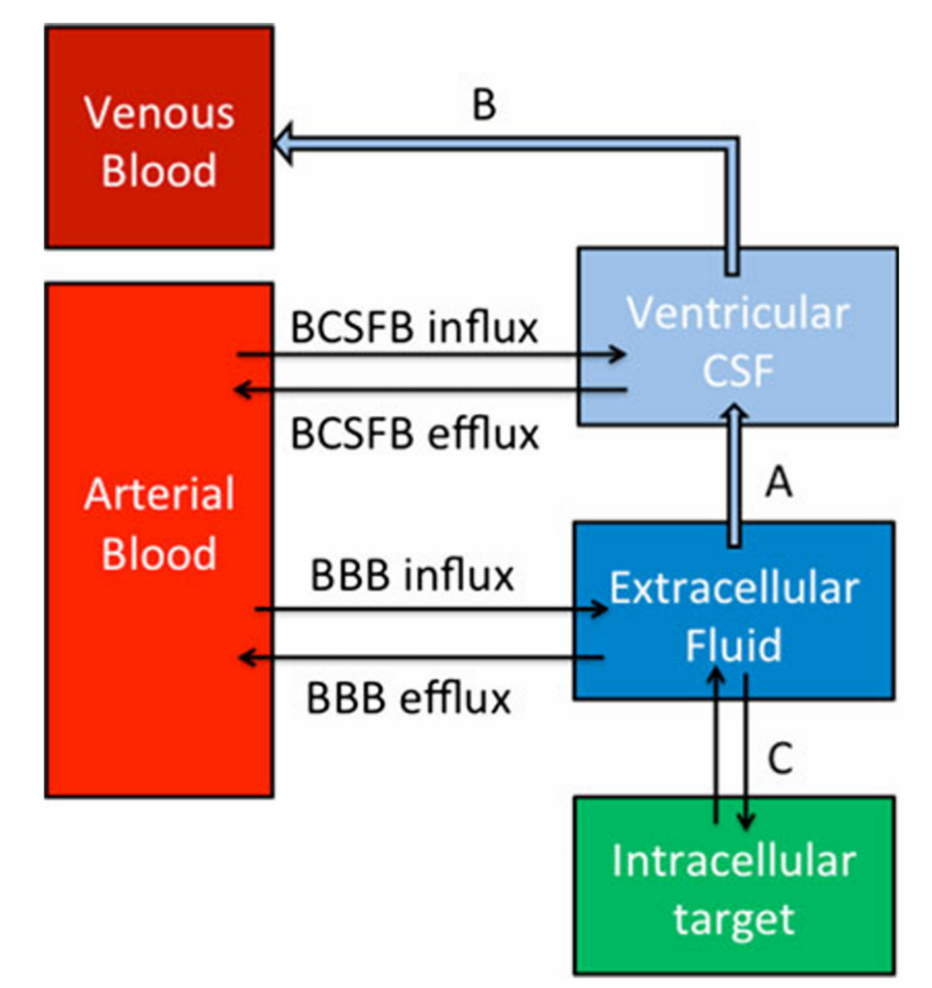
图5 药物在中枢神经系统(CNS)中分布的关键路径与屏障[9]
图 5 展示了药物从血液循环进入中枢神经系统不同腔室的动态转运过程,呈现了药物入脑必须跨越的两大核心屏障(血脑屏障与血脑脊液屏障)及其各腔室间的物质交换关系。
传统研究常以脑脊液(CSF)药物浓度替代脑内游离浓度,该方法虽简便,但对于外排转运体底物药物,CSF浓度可能导致对脑内浓度的错误估计。脑微透析技术可同步监测脑内药物浓度变化并采集系列血样,从而精确阐明血浆PK与靶区浓度之间的关联。
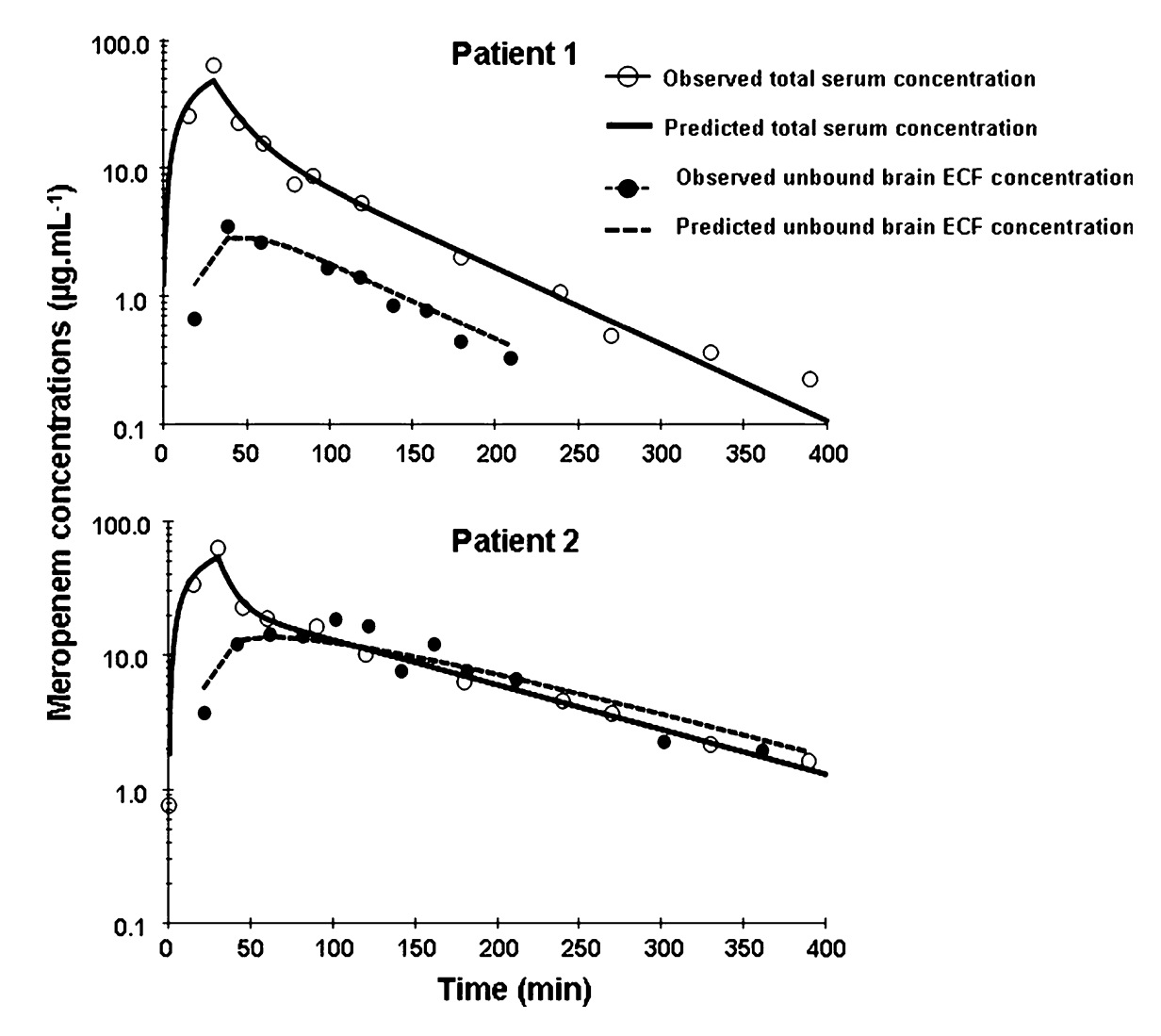 图6 同步脑微透析与血液采样获得的浓度-时间曲线[9]
图6 同步脑微透析与血液采样获得的浓度-时间曲线[9]
通过植入脑组织的微透析导管持续采集脑细胞外液中的游离药物,并同步采集静脉血测定血液总药物浓度,从而构建药物在血液与脑内的浓度-时间曲线,获取AUC、Kp,uu等关键药动学参数。该方法不仅能评估药物透过血脑屏障的能力,还可同步监测脑内内源性物质的动态变化,实现对药物脑内药动学特征的全面分析[9]
2、血液微透析
传统的取血方式(如静脉采血,眼球采血,尾静脉采血)较为常用,但血液成分复杂,含有多种内源性物质进行干扰,其操作繁琐,取样后还需进行分离净化等步骤,且所需的实验动物量大,不能维持实验体正常的生理活动。血液微透析技术由于其膜的选择透过性和不损耗体液流失的特点,可提供不含蛋白质、酶等大分子物质的样品还避免了酶降解,提高了样品的稳定性。因此,微透析技术非常适用于药代动力学、药效学及整合PK-PD研究。
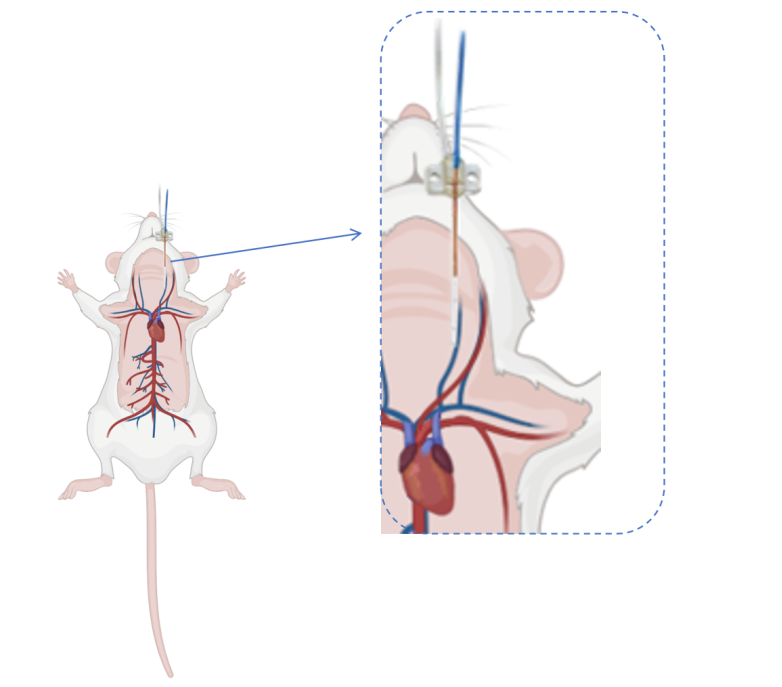
图7 静脉插管(血液)微透析示意图
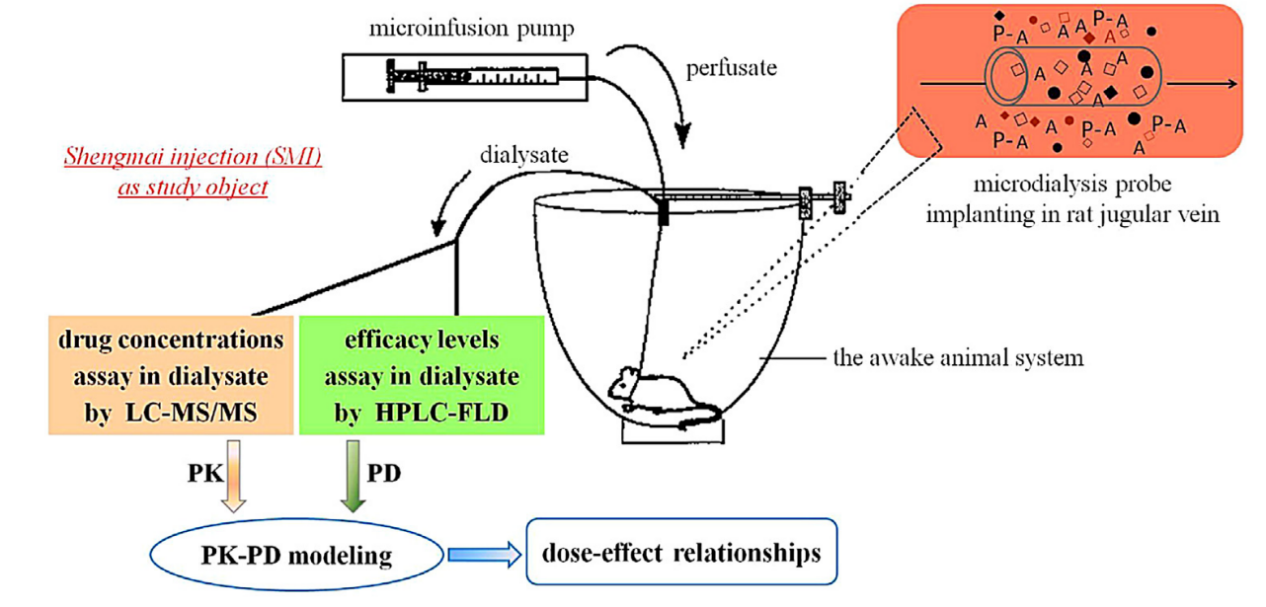 图8 血液微透析在PK-PD建模中的应用示例
图8 血液微透析在PK-PD建模中的应用示例
3、脑部-血液同步微透析
通过在脑组织与血管中同步植入探针,可同时测定BBB两侧游离药物浓度,并评估其平衡过程。该方法消除了个体差异的影响,能准确比较药物在脑与血浆中的动态变化,从而判断药物从脑内排出的速率是否受限。
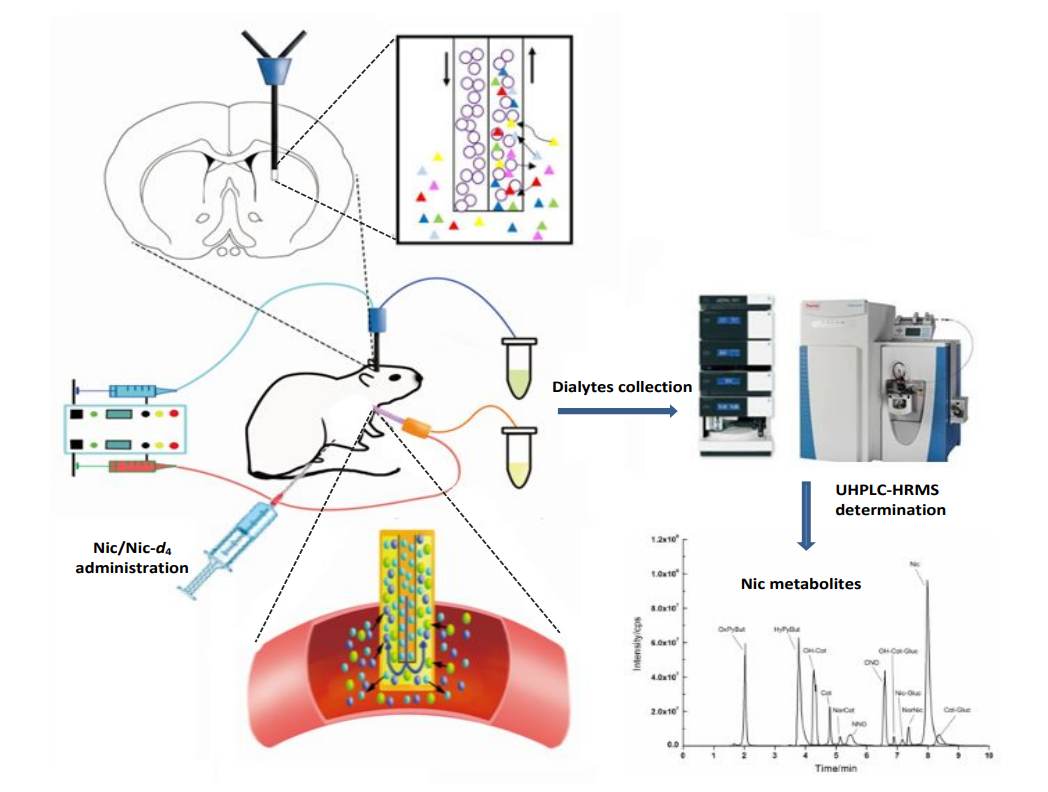
图9 脑部和血液同步微透析示意图
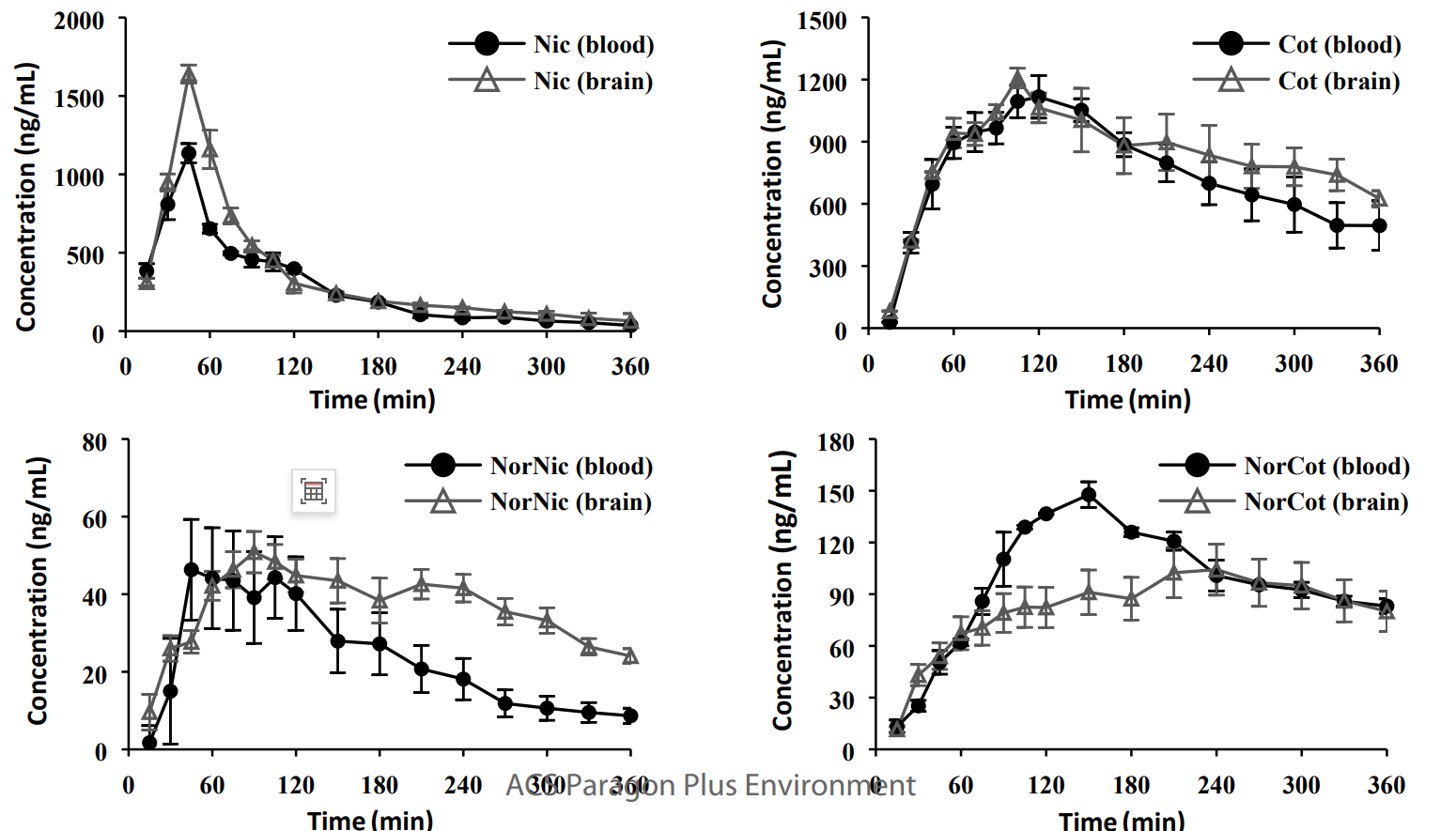
图10 同步微透析技术验证示例
图中显示,尼古丁各代谢物在大鼠脑与血液中的浓度、达峰时间和消除速率均存在显著差异,同步微透析实现了脑血活体同步动态采样,消除了实验误差,直观呈现二者代谢差异,为证实脑内局部代谢、解析尼古丁中枢与外周代谢机制提供了精准的活体数据支撑。
4、皮肤微透析
皮肤微透析以皮肤为靶组织,可动态监测动物或离体皮肤中药物的浓度变化,获取局部药动学参数,并可联合体外实验探索药物的浓度-效应关系。在皮肤病模型中,该方法还能同时监测皮肤不同部位的成分变化,评估屏障功能与药物渗透性的改变。
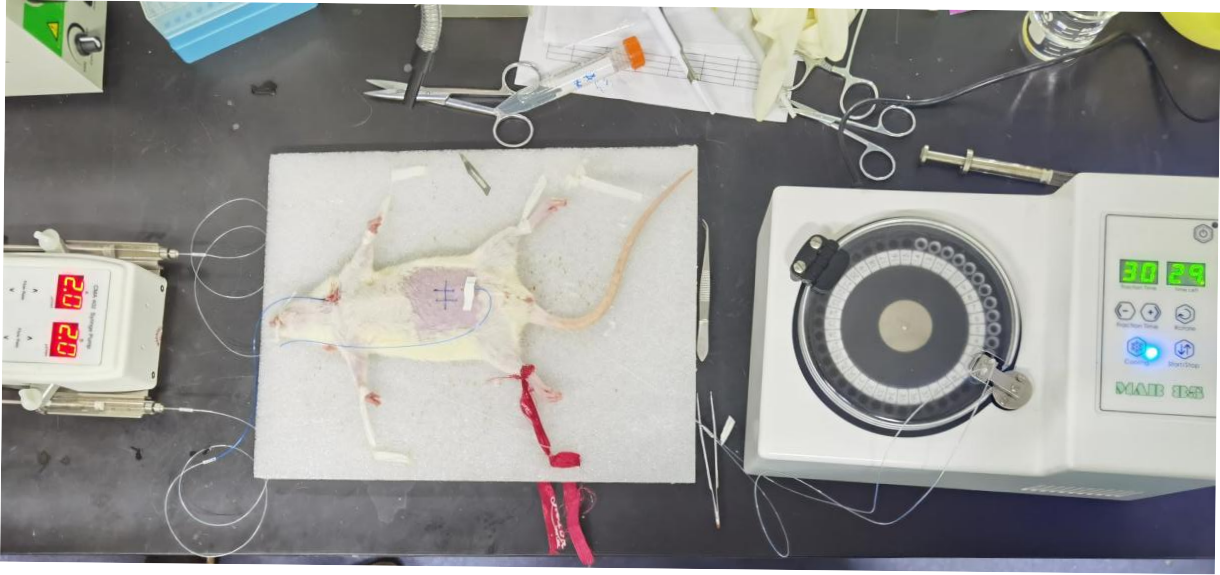 图11 血液-皮肤同步微透析实验示意图
图11 血液-皮肤同步微透析实验示意图
如图11所示,血液与皮肤同步微透析技术,能在同一实验对象体内实现血液、皮肤组织液的同步动态取样——既可以实时追踪药物在血液中的游离浓度变化,又能精准捕捉药物在皮肤局部组织液中的分布、渗透过程,避免了传统分别取样带来的个体差异干。
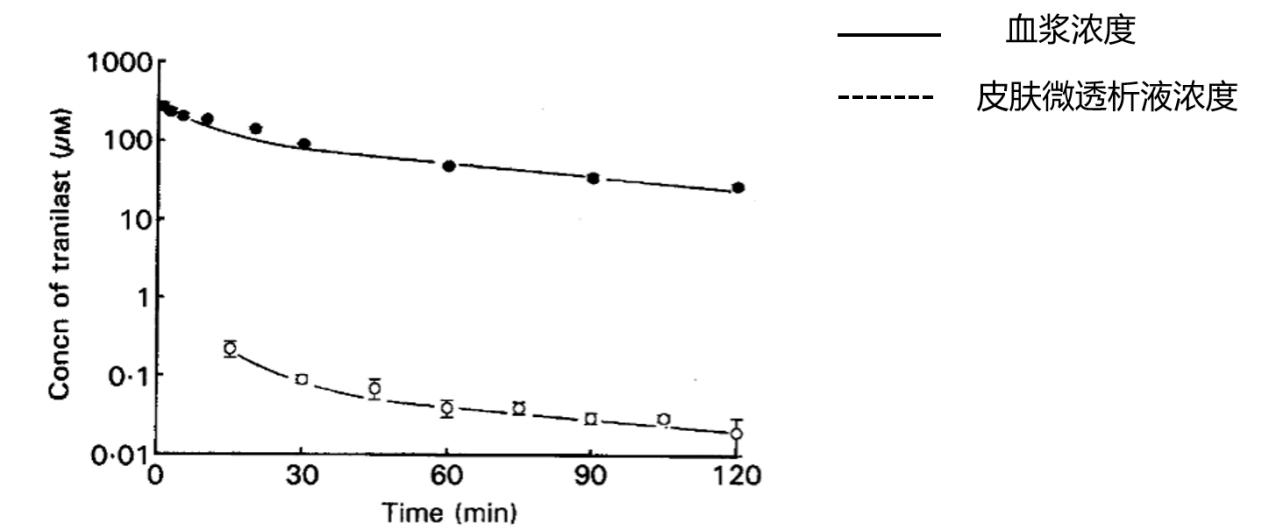 图12 血液与皮肤微透析联用数据[11]
图12 血液与皮肤微透析联用数据[11]
图12研究结果显示,静脉注射后血浆药物浓度迅速达峰并呈双指数衰减,而皮肤组织中药物浓度显著较低且保持稳定。这说明仅凭血液浓度难以准确评估皮肤局部药物暴露水平,凸显了皮肤微透析在局部药动学研究中的重要性。
5、肺部微透析
传统肺部药物浓度监测方法(如痰液、支气管分泌物采集)难以真实反映药物在肺实质中的浓度,尤其对于存在血-肺泡屏障的药物。微透析技术能准确定位于肺靶组织,直接收集游离药物,已成为研究抗菌药物等在肺部药动学的理想工具。
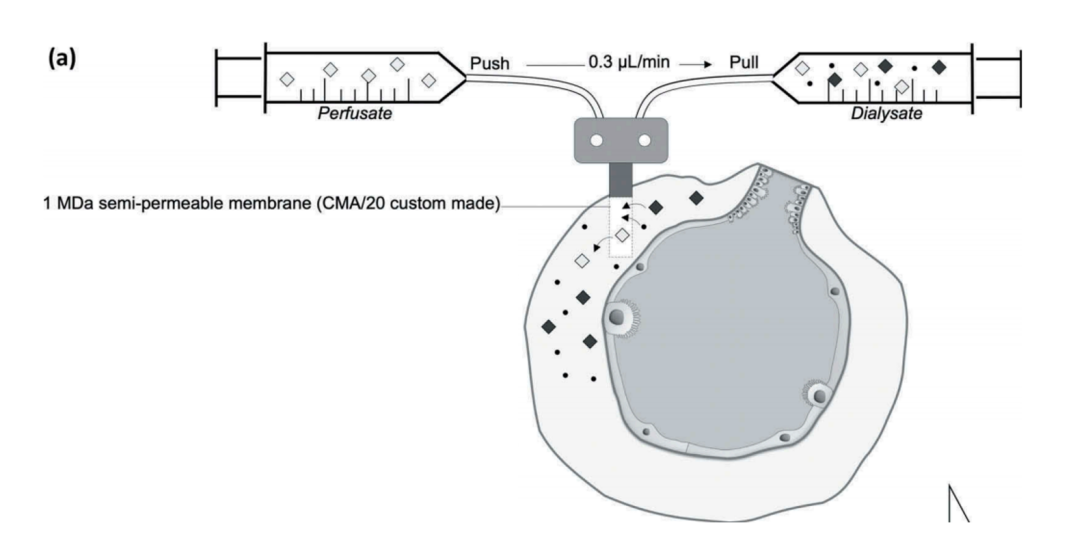
图13肺微透析采样示意图
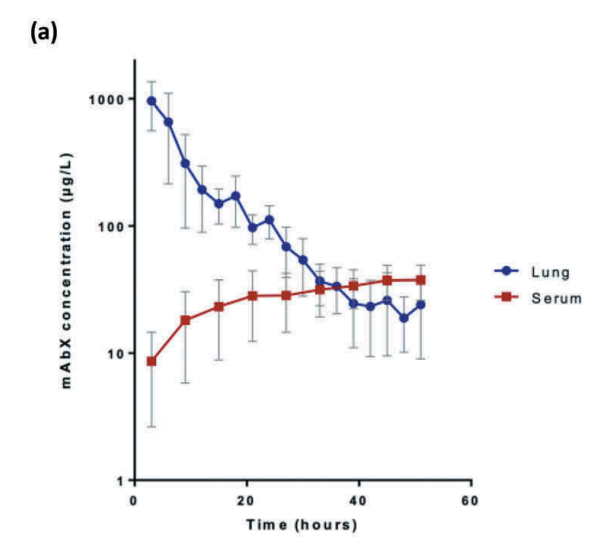
图14 单克隆抗体(mAbX)在肺与血清中的PK曲线
图14结果说明,利用微透析技术可以探索吸入单克隆抗体在肺实质中的命运,二者的连用更实现了对吸入大分子抗体在靶组织(肺)中药代动力学的直接、动态监测[12]。
微透析技术的展望与挑战
当前所处的精准医学时代,神经递质的动态变化与信号转导机制日益成为研究的核心。为了从微观层面深入揭示神经系统疾病在生理及病理状态下的调控网络,必须实时解析这些活性分子在特定脑区内的释放与代谢规律。常规微透析探针主要适用于水溶性小分子,而针对疏水性或易与管路发生非特异性结合的物质,即便通过调整膜材质或降低流速,采样的回收率依然难以令人满意,且易引入偏差。因此,针对不同理化性质的待测物,必须制定个性化的采样方案,通过优化探针参数及管路处理等手段,最大限度减少非特异性吸附和膜透过率差异带来的干扰,从而确保测定结果的真实性与可靠性。
结语
在药物成药性评价中,微透析技术发挥着关键作用。利用该技术能够直接获取靶部位组织中游离态药物,从而开展精准的药代动力学分析。此外,微透析技术不仅局限于体内采样监测,还可作为局部药物递送的载体,为新药研发过程中的递送策略提供创新支持。北京铭泰佳信科技有限公司已成功构建并优化了微透析技术平台,凭借成熟的实验体系和丰富的操作经验,能够全面开展多种组织器官特定区域的游离药物浓度测定及相关药代动力学研究。
参考文献
[1] Azeredo FJ,Dalla Costa T,Derendorf H. Role of microdialysis in pharmacokinetics and pharmacodynamics: current status and future directions. Clin Pharmacokinet. 2014;53 (3):205-212. doi:10.1007/s40262-014-0131-8
[2] Müller, ,Bashaw, ,Bullock, et al.(2007). AAPS-FDA workshop white paper: microdialysis principles, application and regulatory perspectives. Pharmaceutical research, 24 (5), 1014-25. https://doi.org/10.1007/s11095-006-9206-z
[3] 徐铭,李范珠.微透析取样技术及其在体内药物分析中的应用[J].药物分析杂志,2006,(07):1030-1034.DOI:10.16155/j.0254-1793.2006.07.046.
[4] Stangler LA,Kouzani A,Dumee L,et al. Microdialysis and microperfusion electrodes in neurologic disease monitoring Fluids Barriers CNS. 2021 Dec 1;18 (1):52. doi:10.1186/s12987-021-00292-x. PMID:34852829
[5] Zhuang, ,Derendorf, ,Li, ,Xia, ,Gu, , & Liu, (2015). Theory and Application of Microdialysis in Pharmacokinetic Studies. Current drug metabolism, 16 (10), 919-31. https://doi.org/10.2174/1389200216666150812124109
[6] Diab SD,Passmore MR,Fauzi MH,et al. Unintended Consequences: Fluid Resuscitation Worsens Shock in an Ovine Model of Endotoxemia Am J Respir Crit Care Med. 2018 Oct 15;198 (8):1043-1054. doi:10.1164/rccm.201801-0064OC. PMID:29882682
[7] Oddo M,Hutchinson PJ. Understanding and monitoring brain injury: the role of cerebral microdialysis Intensive Care Med. 2018 undefined;44 (11):1945-1948. doi:10.1007/s00134-017-5031-6. PMID:29275512
[8] Reichel A,Feng B,Shaffer C,Lesuisse D,Hoppe E,Fischer H,Di L,Colclough N,Maurer TS,Loryan I. Unbound Brain-to-Plasma Partition Coefficient, K p,uu,brain -a Game Changing Parameter for CNS Drug Discovery and Development Pharm Res. 2022 undefined;39 (7):1321-1341. doi:10.1007/s11095-022-03246-6. PMID:35411506
[9] Carpenter KL,Guilfoyle MR,Helmy A,Hutchinson PJ,Shannon RJ. Cerebral microdialysis in clinical studies of drugs: pharmacokinetic applications J Pharmacokinet Pharmacodyn. 2013 undefined;40 (3):343-58. doi:10.1007/s10928-013-9306-4. PMID:23468415
[10] Xu Y,Zhang Q,Liu J,Chai G,Lu B,Zhang W,Li P,Hong G,Wang D,Zhou H. Nicotine Pharmacokinetics in Rat Brain and Blood by Simultaneous Microdialysis, Stable-Isotope Labeling, and UHPLC-HRMS: Determination of Nicotine Metabolites Anal Chem. 2019 Feb 19;91 (4):2916-2922. doi:10.1021/acs.analchem.8b05078. PMID:30657674
[11] Xu Y,Zhang Q,Liu J,Chai G,Lu B,Zhang W,Li P,Hong G,Wang D,Zhou H. Nicotine Pharmacokinetics in Rat Brain and Blood by Simultaneous Microdialysis, Stable-Isotope Labeling, and UHPLC-HRMS: Determination of Nicotine Metabolites Anal Chem. 2019 Feb 19;91 (4):2916-2922. doi:10.1021/acs.analchem.8b05078. PMID:30657674
[12] Guillon A,Pardessus J,Lhommet P,Parent C,Marchand D,De Monte M,Boixel C,Audat H,Guillot E,Heuze-Vourc'h N. Exploring the fate of inhaled monoclonal antibody in the lung parenchyma by microdialysis MAbs. 2019 undefined;11 (2):297-304. doi:10.1080/19420862.2018.1556081. PMID:30714473